.jpg)
En 1964, Boyd rush se convertía en el primer hombre en someterse a xenotrasplante, recibiendo un corazón de chimpancé que latió unos minutos. Veinte años más tarde, en 1984, una lactante conocida como Baby Fae sería el caso más mediático hasta el momento, reabriendo el debate, científico y ético, del trasplante de órganos de donante animal a receptor humano. El equipo del entonces jefe del Departamento de Cirugía Cardiovascular, Leonard Bailey, del Centro Médico Universitario Loma Linda, en Estados Unidos, uno de los de mayor experiencia mundial en trasplantes pediátricos, injertaba en la niña -que presentaba un síndrome de hipoplasia de corazón izquierdo-, el corazón de un babuino. Baby Fae vivió durante 21 días, dos semanas más que cualquier otro receptor anterior de trasplante de corazón de babuino.
Estos casos subrayan que la perspectiva de utilizar órganos procedentes de animales en humanos como puente a la espera de un órgano definitivo humano no es un hecho novedoso. Pero, también ponen de manifiesto que los científicos estaban a décadas de poder secuenciar el genoma humano, realizar la edición de genes y, mucho menos editarlo con CRISPR-Cas9; avances tecnológicos que han permitido el resurgimiento del xenotrasplante.
Han sido necesarias, pues, más de tres décadas para que por fin se consiguieran culminar un trasplante xenógeno de cerdo a humano. El órgano estaba modificado genéticamente para evitar el rechazo inmediato. El paciente, un varón de 57 años con una enfermedad cardíaca terminal sin más opciones terapéuticas, sigue vivo, camino de cumplir los dos meses desde la intervención, que se llevó a cabo el 7 de enero en la Universidad de Maryland, en Baltimore.
Todavía se tienen pocos detalles sobre la intervención, más allá de las comunicaciones a la prensa, si bien sus responsables han manifestado la intención de publicarlos por los canales científicos habituales. Sí se sabe que la agencia del medicamento estadounidense FDA otorgó la autorización de emergencia para la cirugía en Nochevieja a través de su disposición de uso compasivo. En este caso, el producto médico experimental era el corazón de cerdo modificado genéticamente, considerado por los médicos la única opción disponible para salvar la vida de este paciente.
El proceso de humanización del corazón porcino estuvo a cargo de la compañía biotecnológica estadounidense Revivicor. “Ha sido una cirugía revolucionaria y nos acerca un paso más a la solución de la crisis de escasez de órganos. Simplemente, no hay suficientes corazones humanos de donantes disponibles para cumplir con la larga lista de receptores potenciales”, afirmaba cuando saltó la noticia Bartley P. Griffith, un renombrado cirujano torácico estadounidense y el médico que colocó el corazón de cerdo en el paciente. “Somos optimistas de que esta primera cirugía en el mundo brindará una nueva e importante opción para los pacientes en el futuro”.
Considerado uno de los principales expertos del mundo en xenotrasplante, Muhammad M. Mohiuddin, profesor de cirugía en Maryland, y otro artífice de esta operación pionera, destacó que el caso ha sido “la culminación de años de investigación muy complicada para perfeccionar la técnica en animales con tiempos de supervivencia que superan los nueve meses”. Para el paciente, David Bennett, la decisión de participar en este ensayo estaba clara: “Era morir o hacer este trasplante. Quiero vivir. Sé que es un tiro en la oscuridad, pero es mi última opción”. Llevaba meses postrado en cama del hospital y desde hacía seis semanas, estaba conectado a una máquina de derivación cardiopulmonar (oxigenación por membrana extracorpórea o ECMO). “Espero levantarme de la cama después de recuperarme”.
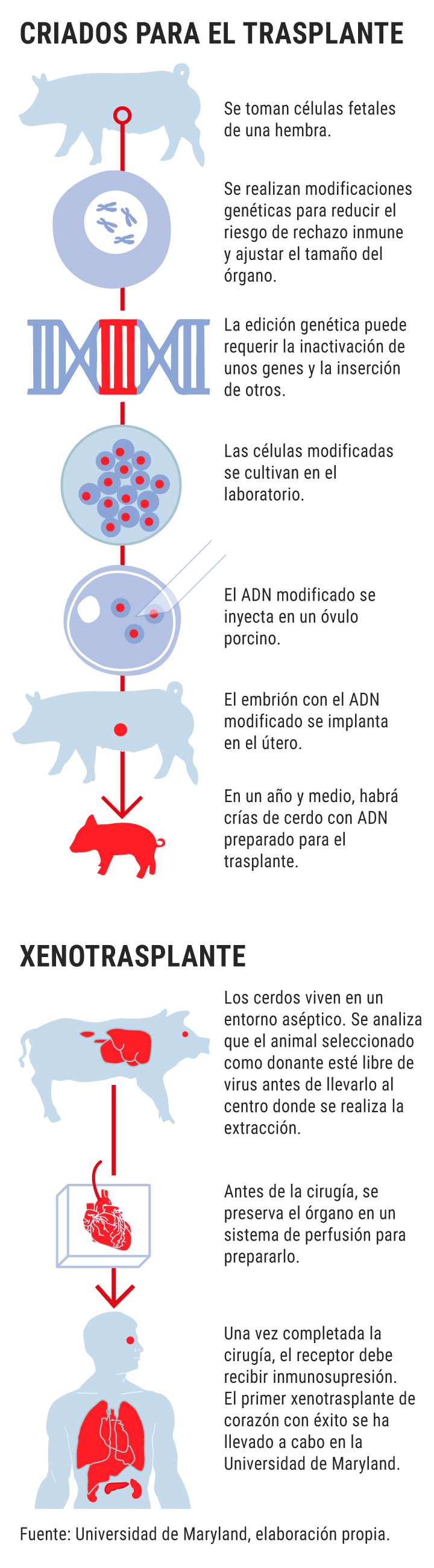
Revivicor, una compañía de medicina regenerativa con sede en Blacksburg (Virginia), proporcionó el órgano de un animal en el que habían realizado diez modificaciones genéticas: se eliminaron tres genes que generan la respuesta inmunitaria mediada por anticuerpos en el ser humano; se introdujo en el genoma del animal seis genes humanos implicados en la tolerancia inmune, y se suprimió un gen que evita el crecimiento excesivo del tejido cardíaco porcino.
.jpg)
Dos equipos de cirujanos efectuaron la extracción y el injerto, dirigidos respectivamente por Mohiuddin y Griffith. Antes del implante, colocaron el corazón animal en un dispositivo de perfusión. Después de ocho horas de cirugía, el paciente ya tenía un nuevo corazón y también un tratamiento inmunosupresor especial. Ha transcendido que se le administra un fármaco experimental (desarrollado por Kiniksa Pharmaceuticals) junto con los medicamentos inmunosupresores convencionales.
Xenotrasplantes renales
Este hito de los trasplantes llega abonado por otro caso de gran repercusión mediática aunque probablemente poco calado científico. A finales de octubre pasado se comunicó mediante una nota de prensa que se había injertado un riñón porcino en un humano en muerte cerebral y con disfunción renal. El órgano, procedente también de las granjas de cerdos de Revivicor, se mantuvo funcional durante tres días, según expusieron los responsables de esta intervención, en el NYU Langone Health de Nueva York. Esa experiencia todavía no se ha publicado en una revista científica. En cambio, apenas dos semanas después del xenotrasplante cardíaco de Maryland, la revista American Journal of Transplantation publicó otro caso similar al neoyorkino: un injerto renal bilateral de cerdo a un hombre que estaba en muerte cerebral.
El equipo quirúrgico responsable de esta intervención, de la Universidad de Alabama (UAB) en Birmingham, realizó el trasplante el 30 de septiembre de 2021 para comprobar su viabilidad. Los riñones porcinos no causaron rechazo hiperagudo, mantuvieron el flujo sanguíneo y produjeron orina hasta que concluyó el estudio, a las 77 horas del injerto.
Jayme Locke, cirujana de trasplantes de la UAB, responsable de la intervención y primera autora de la publicación científica bautizó el procedimiento utilizado como “modelo Parsons”, en honor del receptor del xenotrasplante, James Parsons, y a su familia. De nuevo, los riñones porcinos empleados procedían de Revivicor.
Rafael Máñez, jefe del Servicio de Medicina Intensiva del Hospital Universitario de Bellvitge, ha seguido de cerca estos trabajos. Además de trabajar en un centro puntero en trasplantes cardíacos y renales, en 2000 dirigía una línea de investigación centrada en xenotrasplante en la Unidad de Cirugía Experimental del entonces Hospital Universitario Juan Canalejo (hoy Complejo Hospitalario Universitario de A Coruña); de 2000 a 2003, practicó 20 injertos renales de cerdo transgénico a babuino, logrando una supervivencia de los xenoinjertos de entre 1 y 31 días. Además de situarle como un referente internacional, esas investigaciones han sido la base para ampliar el conocimiento sobre los anticuerpos xenogénicos y, entre otras aplicaciones, desarrollar un tratamiento para mejorar la duración del tejido de origen animal, en concreto, de las válvulas cardíacas.
“No considero que las experiencias que se han conocido sobre el xenotrasplante renal a pacientes en coma aporten mucho desde un punto de vista científico. Confirman que no hay rechazo hiperagudo, pero esto es algo que nosotros ya sabíamos cómo controlar; en cambio no avanzan para averiguar si el xenoinjerto funciona durante un periodo de tiempo prolongado”. Máñez recuerda que además que ya en 2018, se publicó en Journal of American Transplantation un estudio que mostraba que los riñones de cerdos podían funcionar más de un año injertados en primates no humanos, y otro en Nature, con corazones porcinos en primates que se mantenían funcionales más de seis meses funcionales. Este último trabajo, llevado a cabo en colaboración con el equipo de Bruno Reichart, en el Centro de Medicina Experimental Walter Brendel de la Universidad de Múnich, “se topó con el fenómeno de la hipertrofia de los corazones. Hay que tener en cuenta que la tensión arterial sistólica del cerdo ronda los 80 mm Hg, cuando en el mono es como la humana, más elevada; al someter el órgano a una mayor presión, el corazón se hipertrofia. De ahí que en el reciente xenotrasplante cardíaco de Maryland se haya trabajado con corazones en los que se inhibió la hormona del crecimiento”.
Máñez que coincidió con el cirujano cardíaco Griffith durante sus años de estancia en Pittsburgh, aplaude el trabajo del grupo estadounidense, a falta de conocer los detalles del procedimiento, que aún no se han publicado en una revista científica. “Vale la pena que se empiece a probar a estos órganos en el ámbito clínico y poder encontrar una inmunosupresión tolerable a largo plazo y, sobre todo, analizar cómo es la adaptabilidad fisiológico de los órganos de cerdo al entorno humano”.
La clave para que ahora estos intentos tengan más posibilidades de llegar a buen puerto reside, a juicio del especialista, “en la edición genética con CRISPR, en cuyo desarrolló ha sido tan importante el catedrático de Microbiología de la Universidad de Alicante Francisco Juan Martínez Mojica”. El especialista especula que uno de los genes que han silenciado es ara alfa-gal y “probablemente, el del retrovirus endógeno porcino, por su capacidad para infectar células humanas. También es posible que entre los transgenes, se haya introducido algún regulador del complemento”.
Al margen de las posibilidades futuras de los xenotrasplantes, teniendo en cuenta los múltiples obstáculos inmunológicos, biológicos y de compatibilidad, existe un panorama de oferta y demanda entre las necesidades reales de millones de enfermos, afectados de múltiples enfermedades, cuya única salida terapéutica actual se basa en recibir un órgano sano.
José Ramón Núñez, profesor titular de Cirugía de la Universidad Complutense de Madrid (UCM), y hasta 2019, director médico del Programa de Trasplantes de la Organización Mundial de la Salud (OMS), considera que los xenotrasplantes son factibles y espera que en un medio-largo plazo, se pueda disponer de órganos, y ya no como paso intermedio sino como tratamiento definitivo, lo que “sería un avance espectacular”.
De esta forma, la idea de futuro para el xenotrasplante no es que sea un puente intermedio sino tratamiento definitivo. “Como paso intermedio, podría ser válido para una persona determinada, en un momento concreto. El problema es que todos los años, 900.000 personas en el mundo están esperando un trasplante definitivo”, señala Núñez.
Más de un millón de órganos
La información que maneja de los informes emitidos por la OMS alude a que en los últimos 10 años, el número de trasplantes realizados en el mundo se ha incrementado en casi un 30%, lo que supone que se están realizando alrededor de 150.000 trasplantes anuales de órganos sólidos en todo el mundo. Sin embargo, estas cifras solo suponen entre el 10-12% de las necesidades reales de órganos. Se necesitarían entre 1.000.000 y 1.200.00 órganos al año para satisfacer la demanda anual de órganos.
“Un 90% de enfermos esperan un órgano cada año. Pero, es que además, las necesidades están incrementando por varias razones: las expectativas de vida son cada vez mayores, cada vez se indica más el trasplante, incluso en edades en las que anteriormente ni se planteaba y, los resultados los resultados de este procedimiento médico son cada vez mejores. Resultado: la lista de espera aumenta progresivamente, pero aún falta un 90% de órganos anuales y muchas personas fallecen en el camino de la espera del definitivo”, señala Núñez.
Pablo Ramírez, jefe del Servicio de Cirugía General y de Aparato Digestivo y de Trasplante Hepático del Hospital Virgen de La Arrixaca, de Murcia , y director científico del Instituto Murciano de Investigación Biosanitaria (IMIB), de la red del Instituto de Salud Carlos III (ISCIII), considera que los progresos tecnológicos, como la técnica CRISPR, han permitido crear, en poco tiempo, cerdos politransgénicos, frente a los muchos años que anteriormente se tardaba en desarrollar un cerdo con 2 ó 3 genes. “Este hecho ha sido decisivo, incluso ya hay cerdos con más de 60 genes humanos”.
Xenotrasplante hepático en primate
Pero, lo que realmente califica de hito para la medicina ha sido el trasplante cardíaco de un órgano de cerdo con varios genes a un paciente como uso compasivo, del que “se necesita valoración científica, ya que hasta el momento solo ha sido mediática”, indica Ramírez, cuyo equipo de La Arrixaca, hace 20 años y dirigido entonces por Pascual Parrilla, fue pionero en la realización del primer xenotrasplante hepático de mundo con éxito, trasplantando un hígado de cerdo transgénico a un babuino (primate no humano) dentro de un contexto de ensayo preclínico experimental en el que participaron las Universidades de Murcia, Cambridge, en Reino Unido, y Montpellier, en Francia.
Los datos, que se publicaron en Transplantation en el año 2000, abrieron un interesante debate internacional que ahora parece reabrirse. Algunos escasos centros de investigación, como el de la Universidad de Harvard, en Estados Unidos, con Programas de Xenotrasplante, han visto una nueva oportunidad para incorporar cerdos politransgénicos al programa preclínico que tenían con primates, muy similar al de la experiencia del equipo murciano.
via Noticias de diariomedico.... https://ift.tt/1DTZJxS

No hay comentarios:
Publicar un comentario