
España, gracias al trabajo del personal técnico de la Agencia Española de Medicamentos y productos Sanitarios (Aemps), se convirtió en 2023 en el país europeo que más inspecciones de buena práctica clínica realizo en nombre de la Agencia Europea del Medicamento (EMA). Respecto al año anterior, incrementó un 200% su participación en estas inspecciones, tanto en España, COMO en la UE y en terceros países, con el objetivo de garantizar los derechos, la seguridad, la dignidad y el bienestar de las personas que participan en un ensayo clínico, así como de asegurar la calidad y fiabilidad de los datos obtenidos.
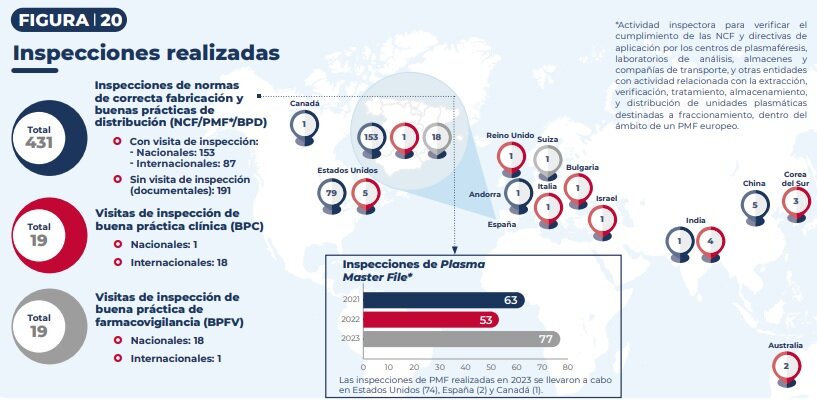
Los inspectores de la Aemps realizaron en 2023 inspecciones en países como Estados Unidos, India, Corea del Sur, Australia o Reino Unido, junto con organizaciones como la FDA o la OMS. En 2023, las inspecciones realizadas de normas de correcta fabricación y buenas prácticas de distribución de Plasma Master File, realizadas a compañías de plasma, aumentaron un 45%, con inspecciones realizadas mayoritariamente en Estados Unidos.
La Agencia subraya que todo este trabajo se une a la labor diaria que desarrolla, de la que la Memoria destaca de 2023 la vigilancia de productos sanitarios, con acciones lideradas por la Aemps gracias a las notificaciones recibidas de los profesionales sanitarios. Estas derivaron en la retirada de productos, como unas lentes intraoculares en todos los países de la UE donde se estaban utilizando.
Igual de decisiva fue la colaboración de estos profesionales en el caso de la farmacovigilancia veterinaria, donde en España se registraron notificaciones de acontecimientos adversos sobre un medicamento llamado florfenicol, que tras su investigación provocó una modificación de la ficha técnica de este antibiótico comercializado en toda la Unión Europea.
La Memoria de Actividades 2023 de la Aemps resume, como todos los años, su actividad basal en números. Destacan los 847 ensayos clínicos y 971 medicamentos autorizados, las 45.318 variaciones resueltas o las 112.076 solicitudes recibidas y evaluadas de medicamentos extranjeros. Un año en que el 1 de julio España asumió la Presidencia del Consejo de la Unión Europea (UE), y que este semestre, según resalta la Agencia, supuso para la Aemps "un verdadero reto, a nivel legislativo, político y técnico, pero también a nivel logístico. Un total de 26 encuentros, incluyendo reuniones de alto nivel, eventos estratégicos y reuniones de trabajo, que contaron con la participación de más de 1.800 representantes de alto nivel y expertos en un total de seis ciudades".
En dicha Memoria se incluyen tres vídeos institucionales: de Mónica García, ministra de Sanidad; de Javier Padilla, secretario de Estado de Sanidad, y de María Jesús Lamas, directora de la Aemps.
García ha resaltado que "no podemos permitirnos que la escasez de principios activos o medicamentos críticos, la falta de instalaciones de fabricación o la fragilidad de las cadenas de suministro lleven a nuestros sistemas sanitarios siempre al límite. Para evitarlo, debemos fortalecer nuestra producción propia y reducir la dependencia de terceros países".
En este sentido, ha destacado el trabajo conjunto del Ministerio de Sanidad y la Aemps: "Durante la pandemia la Aemps llevó a cabo un mapeo de las capacidades productivas españolas para evaluar cómo podrían contribuir a la producción de vacunas", lo que llevó a una "transferencia tecnológica en tiempo récord y un alto rendimiento en producción".
Base de datos BIFAP
Con relación a BIFAP, la mayor base de datos de registros médicos del Sistema Nacional de Salud (SNS) disponible para la investigación y financiada y gestionada por la Aemps, en 2023 ha llegado a los 17,7 millones de historias clínicas anonimizadas disponibles para realizar estudios farmacoepidemiológicos, gracias a la participación de diez comunidades autónomas (Aragón, Asturias, Canarias, Cantabria, Castilla-La Mancha, Castilla y León, Comunidad Valenciana, Madrid, Murcia y Navarra).
via Noticias de diariomedico.... https://ift.tt/5er6Gcp

No hay comentarios:
Publicar un comentario