La multinacional estadounidense Pfizer anuncia que la Agencia Europea de Medicamentos (EMA) ha dado su visto bueno a la autorización de comercialización de sus dos inhibidores de JAK abrocitinib y tofacitinib para dermatitis atópica y espondilitis anquilosante respectivamente. Tras ambas recomendaciones, la Comisión Europea (CE) evaluará los datos y emitirá una decisión próximamente.
En el caso de abrocitinib, el Comité de Medicamentos de Uso Humano (CHMP) ha emitido una opinión positiva recomendando la comercialización de este inhibidor de la Janus quinasa 1 (JAK1) para uso diario en dosis de 100 mg y 200 mg para el tratamiento de la dermatitis atópica de moderada a grave en adultos candidatos a terapia sistémica.
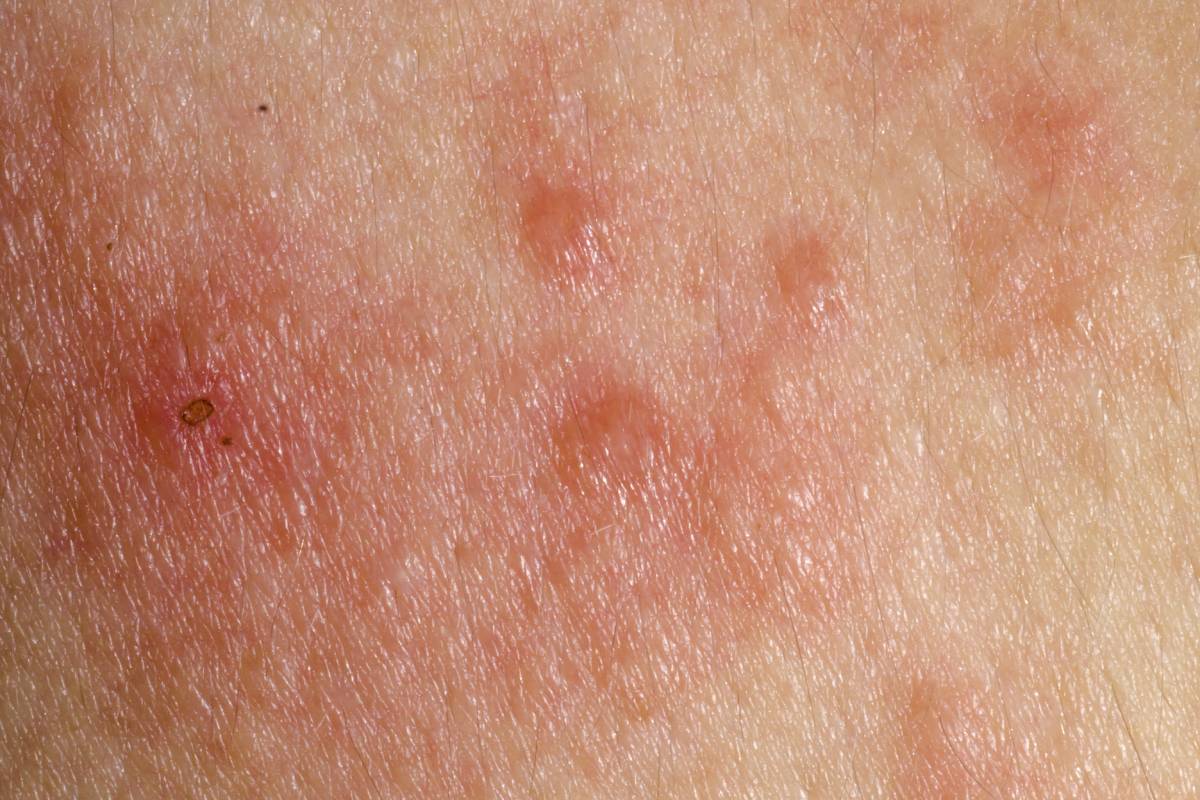
"La dermatitis atópica puede ser una afección debilitante que repercute en la vida cotidiana de millones de personas. Abrocitinib ha demostrado eficacia para combatir esta afección, incluyendo el alivio del picor crónico característico, mejoras en el aclaramiento de la piel, el alcance y la gravedad de la enfermedad frente al placebo, con un perfil favorable beneficio-riesgo. Si finalmente se aprueba, podría convertirse en una nueva e importante opción de tratamiento para los pacientes con dermatitis atópica de moderada a grave", afirma Susana Gómez, directora médica de la Unidad de Inflamación e Inmunología.
Por otro lado, el CHMP también ha emitido una opinión positiva recomendando la autorización de comercialización de una nueva indicación para su medicamento Xeljanz (tofacitinib) de 5 mg y 10 mg dos veces al día para el tratamiento de adultos con espondilitis anquilosante (EA) activa que no hayan respondido adecuadamente a la terapia convencional.
La recomendación de abrocitinib se basa en los resultados de cinco estudios de fase III y un estudio de extensión a largo plazo dentro de un programa de ensayos clínicos que incluye a más de 3.100 pacientes. Por su parte, la recomendación de tofacitinib se basa en los datos de un estudio de fase III, multicéntrico, aleatorizado, doble ciego y controlado con placebo que evaluó la eficacia y seguridad de tofacitinib dos veces al día frente a placebo en 269 pacientes adultos con espondilitis anquilosante activa.
via Noticias de diariomedico.... https://ift.tt/3bbhAMB


No hay comentarios:
Publicar un comentario