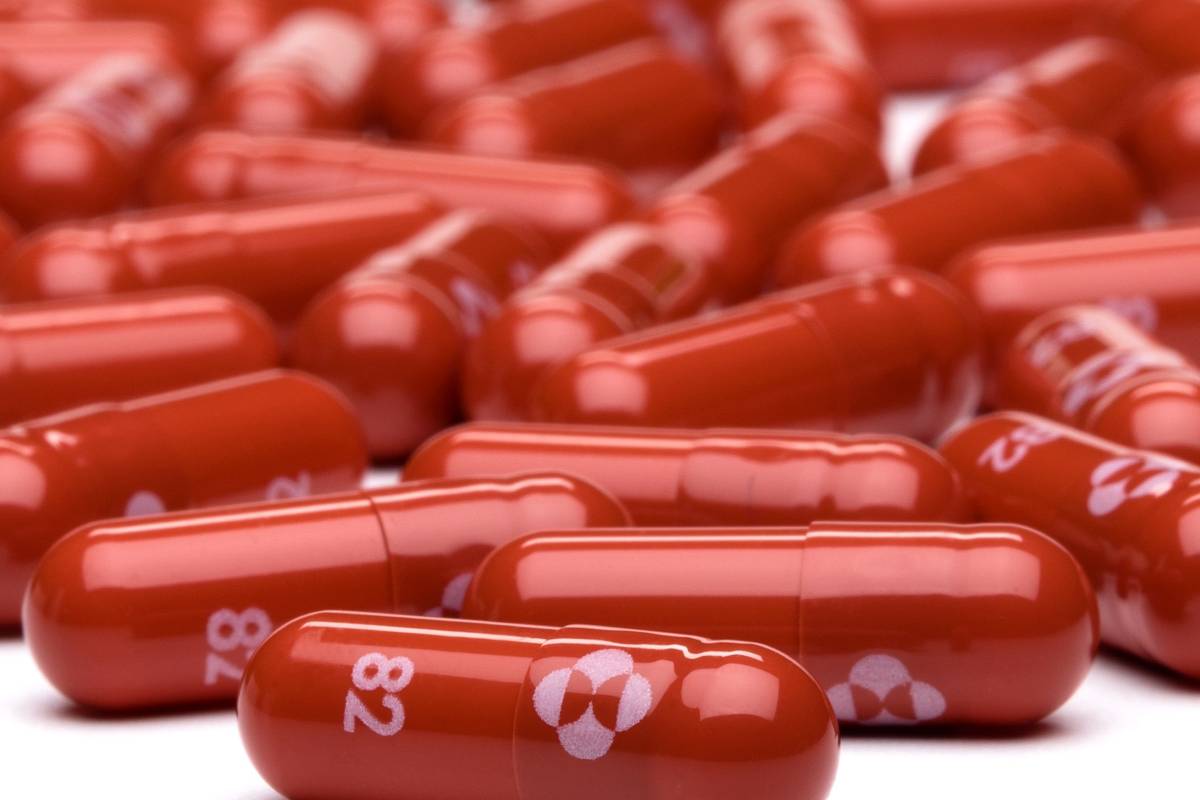
La Agencia Europea del Medicamento (EMA por sus siglas en inglés) abre la puerta al uso de emergencia del antiviral molnupiravir contra la covid-19, desarrollado por las compañías farmacéuticas estadounidenses MSD y Ridgeback Biotherapeutics.
Así lo ha anunciado en rueda de prensa Marco Cavaleri, responsable de Productos Biológicos y Estrategia Vacunal de la EMA.
El organismo europeo está revisando los datos de este fármaco de MSD que, según los datos proporcionados por la compañía farmacéutica, es capaz de reducir a la mitad el riesgo de muerte y hospitalización por covid. Mientras los expertos llegan a una conclusión sobre el medicamento, la EMA ha decidido agilizar el acceso al tratamiento dando vía libre a los estados miembros de la UE para que autoricen su uso bajo la vía de emergencia.
La EMA "está preparada para asesorar a los estados miembros para que puedan hacer que este tratamiento esté disponible para uso de emergencia, antes de que reciba su autorización comercial", ha subrayado Cavaleri, quien ha explicado que la decisión de favorecer el uso de emergencia del fármaco debe interpretarse en el contexto del nuevo incremento de casos que están viviendo la mayoría de países europeos.
Molnupiravir un fármaco antiviral que en el estudio clínico de fase III (en 775 pacientes) ha demostrado reducir el riesgo de hospitalización y muerte en pacientes adultos con covid leve o moderado en un 50% para los no vacunados y para las personas con patologías previas.
La decisión de la EMA coincide con la autorización de molnupiravir por parte de las autoridades reguladoras británicas. Reino Unido es, de momento, el único país que ha aprobado el uso del antiviral.
Aprobación en Reino Unido
La Agencia Reguladora de Medicamentos (MHRA, por sus siglas en inglés) ha anunciado así este jueves que ha dado luz verde a la comercialización de molnupiravir bajo el nombre de Lagevrio. La agencia considera que el medicamento es "seguro y eficaz para reducir el riesgo de ingreso hospitalario y muerte en personas con un covid-19 de leve a moderada que sufren un riesgo adicional".
El ministro británico de Sanidad, Sayid Javid, ha destacado que se trata de un "día histórico" para el Reino Unido, al convertirse en "el primer país en el mundo que aprueba un antiviral para la covid que se puede tomar en casa". Para Javid, supone "un punto de inflexión para los más vulnerables e inmunodeprimidos, que pronto podrán recibir este tratamiento innovador".
Este fármaco está indicado en pacientes positivos con al menos un factor de riesgo de desarrollar enfermedad grave, como obesidad, edad superior a 60 años, diabetes o enfermedad cardiaca. Según los datos de los ensayos clínicos, Lagevrio es más eficaz cuando se toma durante las primeras etapas de la infección, por lo que la MHRA recomienda su uso lo antes posible después de una prueba de SARS-CoV-2 positiva y dentro de los cinco días posteriores al inicio de los síntomas.
via Noticias de diariomedico.... https://ift.tt/3BI1vZv


No hay comentarios:
Publicar un comentario