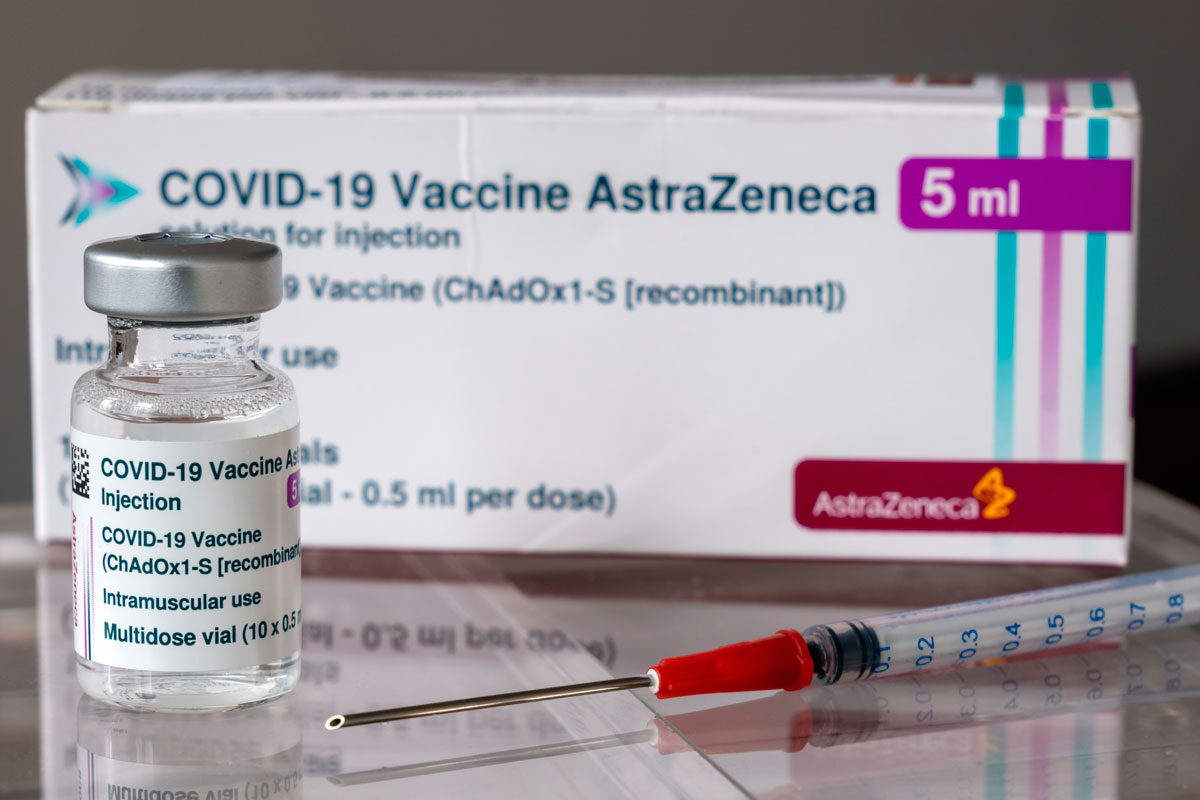
Nuevos datos sobre la vacuna contra la covid de AstraZeneca. Tras finalizar un ensayo en fase III en Estados Unidos, la compañía farmacéutica ha informado en un comunicado que su vacuna no conlleva riesgo de trombos y es eficaz en un 79% a la hora de prevenir casos sintomáticos de covid y en un 100% si se trata de prevenir enfermedad grave y hospitalización.
Los datos, proporcionados por la compañía y que aún no han sido publicados en una revista científica, se basan en el análisis de 32.449 individuos procedentes principalmente de EEUU, aunque también se reclutaron participantes en Perú y Chile. Dos tercios de la muestra recibieron el producto de AstraZeneca, mientras que al resto se le inyectó un placebo. En total, se registraron 141 casos de covid.
AstraZeneca asegura que la eficacia de la vacuna se demostró en todos los grupos étnicos y de edad. De hecho, en la nota subraya que la eficacia de la inmunización en mayores de 65 años, una de las dudas que ha planeado desde hace meses sobre el producto, fue del 80%.
Aproximadamente el 20% de los participantes tenían más de 65 años, detalla el comunicado. De ellos, un 60% presentaba problemas asociados con un mayor riesgo de desarrollar una covid grave, como diabetes, obesidad o enfermedad cardiovascular.
Debido a la preocupación sobre una posible relación con eventos tromboembólicos, la investigación realizó una revisión específica de este aspecto por parte de un comité independiente. Según sus datos, no se encontró ninguna asociación con este tipo de complicaciones, incluida la trombosis venosa cerebral, de la que no se registró ningún caso.
"Estos hallazgos reconfirman resultados previos observados en ensayos con AZD1222 en población adulta, pero es emocionante ver resultados de eficacia similares en personas mayores de 65 años por primera vez", señala Ann Falsey, especialista de la Escuela de Medicina de la Universidad de Rochester y líder de la investigación en el comunicado distribuido por AstraZeneca. Los nuevos datos, añade, confirman que adultos de todas las edades pueden beneficiarse de la protección que confiere la vacuna.
AstraZeneca continuará analizando datos sobre la vacuna y preparando su solicitud de aprobación por parte de la Agencia Estadounidense del Medicamento (FDA por sus siglas en inglés), señala el texto enviado por la compañía, donde también se anuncia la intención de publicar los resultados de estos análisis en una publicación científica revisada por pares.
Seguridad
En cuanto a la administración de la vacuna, la compañía señala que ampliar el intervalo entre las dos dosis necesarias a más de cuatro semanas "podría incrementar la eficacia y acelerar el número de personas que pueden recibir una primera dosis".
El pasado jueves, tras la reunión de su Comité de Farmacovigilancia y Evaluación de Riesgos (PRAC), la Agencia Europea del Medicamento (EMA) ratificó la seguridad de la vacuna y dio luz verde a la administración del producto, que se había suspendido en varios países europeos -incluido España- debido a la notificación de casos de trombosis venosa cerebral en personas que habían recibido la vacuna.
"La vacuna es segura y efectiva en la protección frente a la covid-19, y sus beneficios continúan siendo muy superiores a los posibles riesgos", señaló Sabine Straus, directora del PRAC.
"El número de eventos trombóticos reportados entre la población vacunada -añadió- es menor que el esperado en la población general, según ha observado el comité", por lo que se ha concluido que "no hay un aumento en el riesgo global de aparición de trombos. Sin embargo, aún hay ciertas incertidumbres; hemos visto algunos casos muy raros describiendo una combinación de trombosis, trombocitopenia y hemorragias, en algunos casos empezando por pequeños trombos entre los 7 y los 14 días posteriores a la vacunación, una condición conocida como coagulación intravascular diseminada. También unos pocos casos de trombosis de senos cerebrales. Estas condiciones están relacionadas con una trombocitopenia y aun no hay evidencia científica suficiente para determinar si estos eventos están relacionados con la vacuna, aunque son muy raros, por el PRAC lo seguirá investigando", aseveró.
Tras la decisión de la EMA, el Ministerio de Sanidad decidió levantar la suspensión de la vacuna y anunció que el próximo miércoles se retomará la administración del producto. Está previsto que este lunes el Consejo Interterritorial de Salud decida a qué grupos de edad se administrará la vacuna, que hasta ahora estaba reservada para los menores de 55 años.
La ministra de Sanidad ratificó el pasado jueves el objetivo de vacunar a un 70% de la población antes del final del verano. "Si las compañías cumplen con los contratos, el compromiso se mantiene", ha señalado. La responsable de Sanidad ha apuntado que Janssen comenzará a suministrar su vacuna monodosis en la segunda quincena de abril.
En su intervención del jueves, Darias defendió la paralización de la campaña durante unos días. "Fue una decisión complicada, pero acertada", ha dicho la ministra. "No se suspendió la vacuna, lo que se hizo fue pausar la vacunación hasta tener más datos", apuntó, por su parte, María Jesús Lamas, directora de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). "Yo no creo que esto debilite la confianza en las vacunas", subrayó la máxima responsable de la AEMPS. Desde su punto de vista, este episodio muestra que "el sistema funciona".
Sin embargo, un 52% de los españoles ve ahora la vacuna contra la covid-19 de AstraZeneca como "insegura", frente al 25% que lo hacía en febrero, según una encuesta realizada por YouGov en más de ocho mil personas en Reino Unido, Alemania, Italia, España, Dinamarca y Suecia, informa Europa Press.
via Noticias de diariomedico.... https://ift.tt/2Ph7qCs


No hay comentarios:
Publicar un comentario